Next: 5 Números cuánticos
Up: Tema 2: Estructura atómica
Previous: 3.5 El espectro del
El éxito de la teoría de Bohr condujo al desarrollo posterior de la mecánica
cuántica (MC). Esta es la parte de la Física que se aplica a los sistemas
microscópicos (átomos, núcleos, moléculas, etc).
Según esta teoría las partículas no describen trayectorias definidas
y sólo se puede conocer la probabilidad de encontrar una partícula en
determinada región del espacio. El estado físico se describe por una función
de onda compleja. Por ejemplo, para un electrón en el átomo de H, la
función de onda será una función de 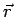 y
y 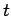
La probabilidad de encontrar alelectrón en un volumen 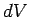 en el punto
en el punto
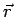 y en el instante
y en el instante 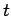 es
es
La probabilidad total debe ser uno, por lo que la integral de volumen
La función de onda se obtiene resolviendo la ecuación de Schroedinger
donde 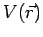 es la energía potencial.
es la energía potencial.
Las órbitas estacionarias clásicas corresponden en MC a ondas estacionarias
del tipo
Resolviendo la ecuación de Schroedinger se obtienen las energías 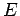 y
funciones de onda
y
funciones de onda 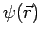 de los estados cuánticos estacionarios.
Para el átomo de H se obtienen las mismas energías que en el modelo de
Bohr. Ahora bien, desde el nuevo punto de vista, el electrón ya no
describe una órbitas, sino que está descrito por la función de onda
de los estados cuánticos estacionarios.
Para el átomo de H se obtienen las mismas energías que en el modelo de
Bohr. Ahora bien, desde el nuevo punto de vista, el electrón ya no
describe una órbitas, sino que está descrito por la función de onda
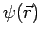 . Por ejemplo, para el nivel
. Por ejemplo, para el nivel 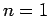 se obtiene
se obtiene
donde 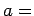 radio de Bohr.
radio de Bohr.



Next: 5 Números cuánticos
Up: Tema 2: Estructura atómica
Previous: 3.5 El espectro del
J.E. Amaro
2006-05-26
![]() y
y ![]()