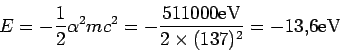Next: 3.4 Energía de ligadura
Up: 3 Modelo atómico de
Previous: 3.2 Radios de las
Primero calculamos la velocidad
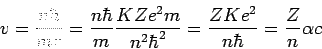 |
(19) |
La energía de la órbita es 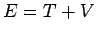 ,
donde la energía cinética es
,
donde la energía cinética es
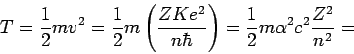 |
(20) |
y la energía potencial
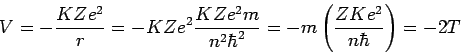 |
(21) |
Por lo tanto la energía total
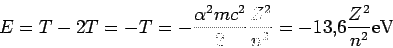 |
(22) |
Ejercicio. Calcular la energía de la primera órbita en el átomo de H
Solución. Para el H, 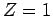 . Para la primera órbita,
. Para la primera órbita, 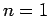
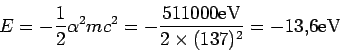 |
(23) |



Next: 3.4 Energía de ligadura
Up: 3 Modelo atómico de
Previous: 3.2 Radios de las
J.E. Amaro
2006-05-26
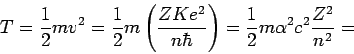
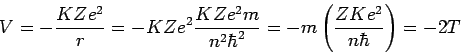
. Para la primera órbita,